Vereinfachung der Wirksamkeitstests von CBD-Fruchtgummis
Vereinfachung der Wirksamkeitstests von CBD-Fruchtgummis
Neues, flexibles Verfahren vereinfacht die genaue Bestimmung des Cannabidiol-Gehalts in Süßigkeiten auf Fruchtgummi-Basis

Das aktuelle und rasche Wachstum der weltweiten Cannabinoid-Branche hat auch zur Einführung von zahlreichen medizinisch wirksamen Lebensmitteln (Nutrazeutika) geführt. Zu den beliebtesten zählen Süßigkeiten auf Fruchtgummi-Basis. Shimadzu nahm eine Reihe von Untersuchungen vor, um zu prüfen, inwieweit derzeit verfügbare Geräte den Gehalt von Cannabidiol (CBD) in Fruchtgummis messen können. Das Extraktionsverfahren wurde durch Standardaddition bewertet, wobei sowohl Gummis ohne Cannabinoid als auch handelsübliche CBD-Fruchtgummis verwendet wurden. Die Tests waren eindeutig: Eine einfache Lösungsmittelextraktion und anschließende HPLC-Analyse mit Detektoren der i-Serie LC-2060 mit Photodiodenarraydetektor (PDA) ist ein sensitives, robustes Verfahren für die exakte Extraktion und Bestimmung des CBD-Gehalts und erfordert nur sehr wenig zusätzliche Laborausrüstung.
HINTERGRUND
In den vergangenen Jahren wurde der Cannabispflanze erneut Aufmerksamkeit zuteil, die meistens positiv ausfiel. Während ihre Verwendung für Medizin- oder Freizeitzwecke weiterhin Gegenstand von Diskussionen ist, sind Produkte, die weniger als 0,2 % des psychoaktiven Wirkstoffs Delta-9-Tetrahydrocannabinol (THC) enthalten, seit langem in vielen Ländern legal.
Infolgedessen ist der Markt für Nahrungsmittel, die Cannabidiol (CBD) enthalten, enorm gewachsen. Dies hat die Anforderungen an die Hersteller für die genaue Bestimmung von Cannabinoiden in ihren Produkten erhöht, z B. für die exakte Etikettierung, Konsumentensicherheit, Qualitätskontrolle und Einhaltung von Bestimmungen. Insbesondere für Produkte, die Süßigkeiten für Kinder gleichen – wie beispielsweise CBD-haltige Gummibären – muss garantiert sein, dass sie keine potenziell toxischen Inhaltsstoffe enthalten.
Entstehung der Studie
Angela Jein, Technikerin für Flüssigchromatographie bei Shimadzu UK, wurde zunehmend bewusst, dass sowohl Hersteller als auch Labore bei der Bestimmung des CBD-Gehalts ihrer Süßwaren vor Herausforderungen standen. Schließlich gelang es Angela trotz der Komplikationen und Einschränkungen durch die Covid-19-Pandemie eine sechsmonatige Studie anzustoßen, wie das CBD-Extraktionsverfahren verbessert werden kann, um den Marktanforderungen besser gerecht werden zu können.
Ziele und Herausforderungen
Ziel: Untersuchung eines neuen, leistungsfähigeren Verfahrens
Das vorrangige Ziel der Studie war es, ein einfaches und dennoch zuverlässiges Verfahren für die Extraktion und Analyse von Cannabinoiden (in CBD-Nutrazeutika) zu finden und zu testen, um es Herstellern und Kontrolllaboren zu erleichtern, die Qualität sicherzustellen.
Aufgabe: Bearbeitung komplexer Grundsubstanzen
Die Analyse von Wirkstoffen in Nahrungsmitteln ist im Allgemeinen immer eine Herausforderung, da Nahrungsmittelproben zahlreiche verschiedene Substanzen enthalten, die den Test beeinflussen können (d. h. die Bestimmung bestimmter Mengen eines definierten Stoffs in einer Lösung). In Süßwaren auf Fruchtgummi-Basis (Abb. 1) sind der hohe Zucker- und Gelatinegehalt eine derartige Herausforderung.
Darüber hinaus haben die neuesten allgemeinen Trends zu weiteren Komplikationen geführt. Cannabinoid-Fruchtgummis haben sich – parallel zur Marktnachfrage nach veganen und zuckerfreien Alternativen – zu konventionellen Produkten entwickelt, die häufig auf Gelatinebasis hergestellt sind und Zucker enthalten.
Um diese Hindernisse zu überwinden, können die betreffenden Analyten am besten exakt bestimmt werden, wenn man ein effektives und selektives Extraktionsverfahren mit einer „Leerwert“-Referenzprobe einer Gummimatrix ohne Cannabinoide kombiniert. Dafür wird der Referenzprobe eine bekannte Konzentration eines Cannabinoid-Standards zugefügt, gefolgt von Extraktion und Quantifizierung. Auf diese Weise können die Wiederfindungsrate und Genauigkeit des Verfahrens genau bestimmt werden.
Ziel: Einrichtung eines wirtschaftlichen Verfahrens
Beim zweiten Ziel lag das Augenmerk auf den praktischen Aspekten des Tests. Laut Angela Jein wird zudem für die wenigen für Nahrungsmittel, Kosmetika und Nutrazeutika verfügbaren CBD-Extraktionsverfahren „im Allgemeinen eine umfangreiche High-Tech-Ausrüstung wie die Tieftemperatur-Probenvorbereitung, automatische Rüttelgeräte, Zentrifugen und Sonstiges benötigt.“ Daher sollte der Test auch dazu dienen, ein robustes Verfahren zu etablieren, bei dem die Extraktion mit einer möglichst einfachen Laborausrüstung zufriedenstellend realisiert werden kann.
Aufgabe: Beschränkung des Bedarfs an zusätzlicher Laborausrüstung
Die Analyse von Esswaren ist für viele Labore, die nicht über die gesamte Palette der üblichen Extraktionsausrüstung wie Zerkleinerer, Zentrifugen, Wasserbäder, mechanische Rüttler, Rotationsverdampfer, usw. verfügen, eine Herausforderung.
Material und Methoden
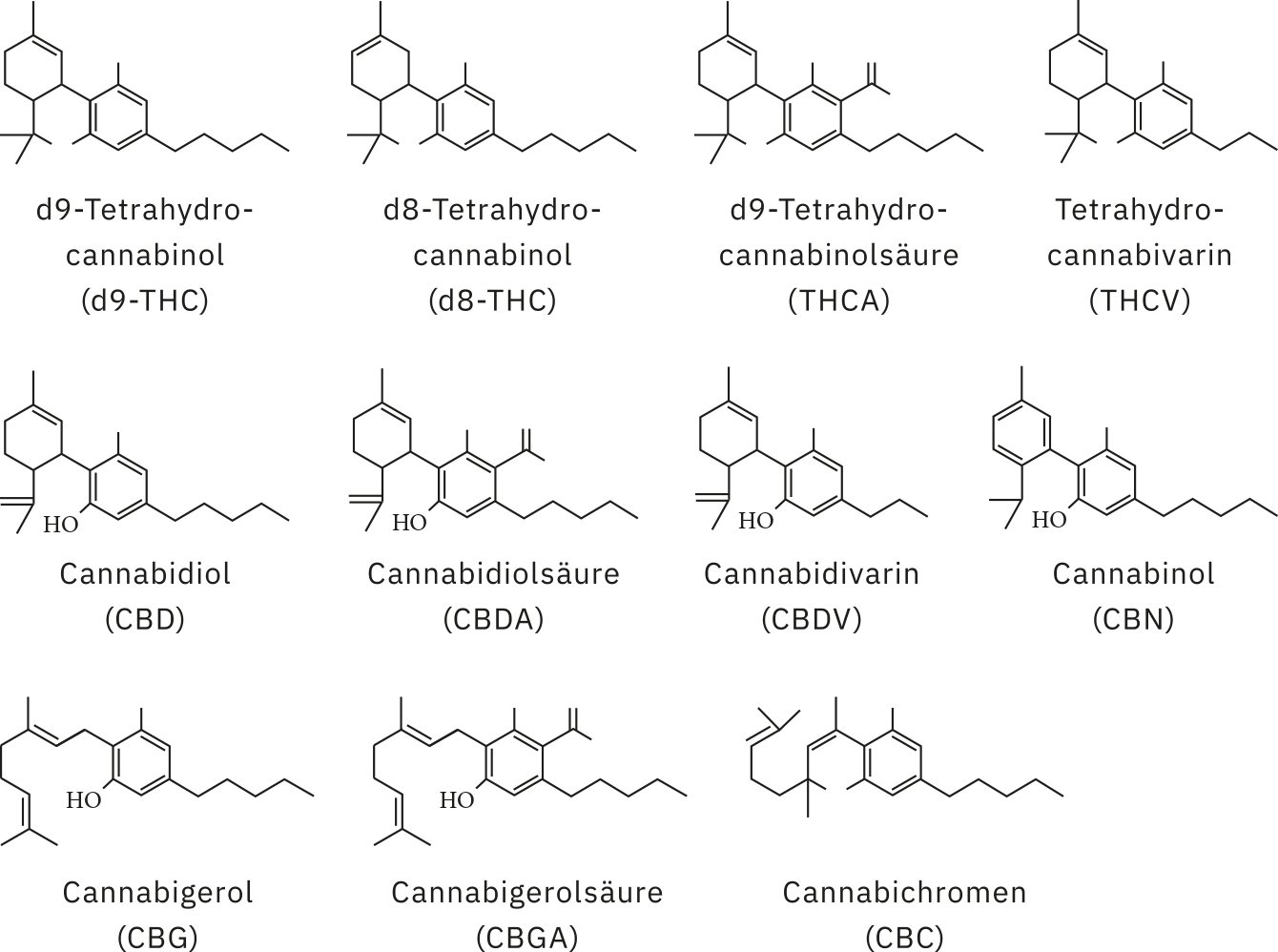
Die Analyse aller Proben wurde mit der hochempfindlichen Methode von Shimadzu für Wirksamkeitstests [1] auf einer LC-2060 mit Photodioden-Array (PDA)-Detektor durchgeführt. Hierbei handelt es sich um ein integriertes Ultrahochleistungs-Flüssigkeitschromatographie-System (UHPLC) der i-Serie. Referenzstandards wurden aus einzelnen Cannabinoid-Standards für einen Konzentrationsbereich von 0,5 bis 90,9 ppm für 11 Cannabinoide hergestellt (Abb. 2): Cannabidivarin (CBDV), Cannabidiolsäure (CBDA), Cannabigerolsäure (CBGA), Cannabigerol (CBG), Cannabidiol (CBD), Tetrahydrocannabidivarin (THCV), Cannabinol (CBN), Δ9-Tetrahydrocannabinol (Δ9-THC), Δ8-Tetrahydrocannabinol (Δ8-THC), Cannabichromen (CBC), Δ9-Tetrahydrocannabinolsäure (THCA).
Probenvorbereitung
Eine CBD Standardlösung (A) mit ca. 100 mg/l wurde aus CBD-Isolat bekannter Reinheit in Methanol hergestellt. Standardlösungen für alle Cannabinoide wurden bereitet, indem man ein bekanntes Volumen jedes Cannabinoids direkt der Probe hinzufügte.
Kontroll-Fruchtgummi ohne Cannabinoide ist auf dem Markt erhältlich und wurde als Leerprobe verwendet, um das Extraktionsverfahren zu validieren. Die Fruchtgummis wurden kleingeschnitten und gründlich zu einer repräsentativen Probe vermischt.
Standardaddition wurde mit bestimmten Mengen an Lösung A oder B durchgeführt, die vor der Extraktion in das Fruchtgummi einziehen konnten (Abb. 3).
Zur Beurteilung der Präzision des Extraktionsverfahrens wurden durch Zugabe von Lösung A sechs Wiederholungsproben mit einer CBD-Endkonzentration von 20 ppm erstellt. Darüber hinaus wurden zwei Proben mit Lösung (B) versetzt, um alle 11 Cannabinoide nach der Extraktion doppelt zu analysieren.
Da handelsübliche CBD-Nahrungsmittel in den unterschiedlichsten Größen und Konzentrationen verkauft werden, wurde die Genauigkeitstestung doppelt bei 5 ppm, 20 ppm und 40 ppm durchgeführt.
Zur Bestimmung der Selektivität des Tests gegen unbekannte Peaks in der Gummimatrix, die möglicherweise den Cannabinoid-Nachweis beeinflussen könnten, wurden die folgenden Referenzproben getestet:
- Durchsichtiges (reines) Gummi / keine Standardaddition
- Rotes (reines) Gummi / keine Standardaddition
- Orangefarbenes (reines) Gummi / keine Standardaddition
- Gelbes (reines) Gummi / keine Standardaddition
- Grünes (reines) Gummi / keine Standardaddition
- Gummi sämtlicher Farben / keine Standardaddition
- Zufällig gefärbtes Gummi / keine Standardaddition
- Kein Gummi vorhanden / Standardaddition
- Kein Gummi vorhanden
Für realitätsnahe Proben wurden drei handelsübliche CBD-Gummiprodukte (vegan und nicht vegan) von zwei unterschiedlichen Herstellern mit dem beschriebenen Verfahren analysiert. Es wurden Unterproben von jedem Typ genommen und kleingeschnitten (< 1/16 Größe). Zur Untersuchung der Robustheit der Proben selbst wurden mehrere Teilproben (8) jeder Probe getestet.
Probe 1 – Nicht-vegan – Hersteller A [bunt]
Probe 2 – Vegan – Hersteller A [bunt]
Probe 3 – Vegan – Hersteller B [nur grün]
Ergebnisse und Diskussion
Tabelle 1 zeigt die Ergebnisse für Präzision, Genauigkeit und Selektivität der Extraktion und Gehaltsbestimmung von CBD in den Referenzproben.
|
Kennzeichnung / Nummer |
CBD-Gehalt (ppm) |
% Nennwert |
|
|
Standardlösung A |
— |
107,2 mg/ml |
— |
|
Präzision |
1 |
19,886 |
98,9 |
|
2 |
19,905 |
99,0 |
|
|
3 |
20,187 |
100,4 |
|
|
4 |
20,254 |
100,8 |
|
|
5 |
19,862 |
98,8 |
|
|
6 |
19,933 |
99,2 |
|
|
Genauigkeit |
1 (25 % Präzision) |
4,984 |
99,2 |
|
2 (25 % Präzision) |
4,930 |
98,1 |
|
|
3 (100 % Präzision) |
20,109 |
100,1 |
|
|
4 (100 % Präzision) |
19,839 |
98,7 |
|
|
5 (200 % Präzision) |
39,821 |
99,1 |
|
|
6 (200 % Präzision) |
40,194 |
100,0 |
|
|
Selektivität |
1 – Durchsichtig / keine Standardaddition |
— |
— |
|
2 – Rot / keine Standardaddition |
— |
— |
|
|
3 – Orange / keine Standardaddition |
— |
— |
|
|
4 – Gelb / keine Standardaddition |
— |
— |
|
|
5 – Grün / keine Standardaddition |
— |
— |
|
|
6 – Alle / keine Standardaddition |
— |
— |
|
|
7 – Gemischt / keine Standardaddition |
— |
— |
|
|
8 – Gemischt / keine Standardaddition |
19,848 |
98,8 |
|
|
9 – Kein Gummi / keine Standardaddition |
— |
— |
|
|
Kennung / statistischer Aspekt |
CBD-Gehalt (ppm) |
% Nennwert |
|
|
Präzision |
Standardabweichung |
20,005 |
99,5 |
|
Durchschnitt |
0,170 |
99,5 |
|
|
% RSD |
0,851 % |
0,851 % |
|
|
Genauigkeit |
Durchschnitt 25 % |
4,957 |
98,7 |
|
Standardabweichung |
0,038 |
0,008 |
|
|
% RSD |
0,770 % |
0,770 % |
|
|
Durchschnitt 100 % |
19,974 |
99,4 |
|
|
Standardabweichung |
0,191 |
0,009 |
|
|
% RSD |
0,956 % |
0,956 % |
|
|
Durchschnitt 200 % |
40,008 |
99,5 |
|
|
Standardabweichung |
0,264 |
0,007 |
|
|
% RSD |
0,659 % |
0,659 % |
|
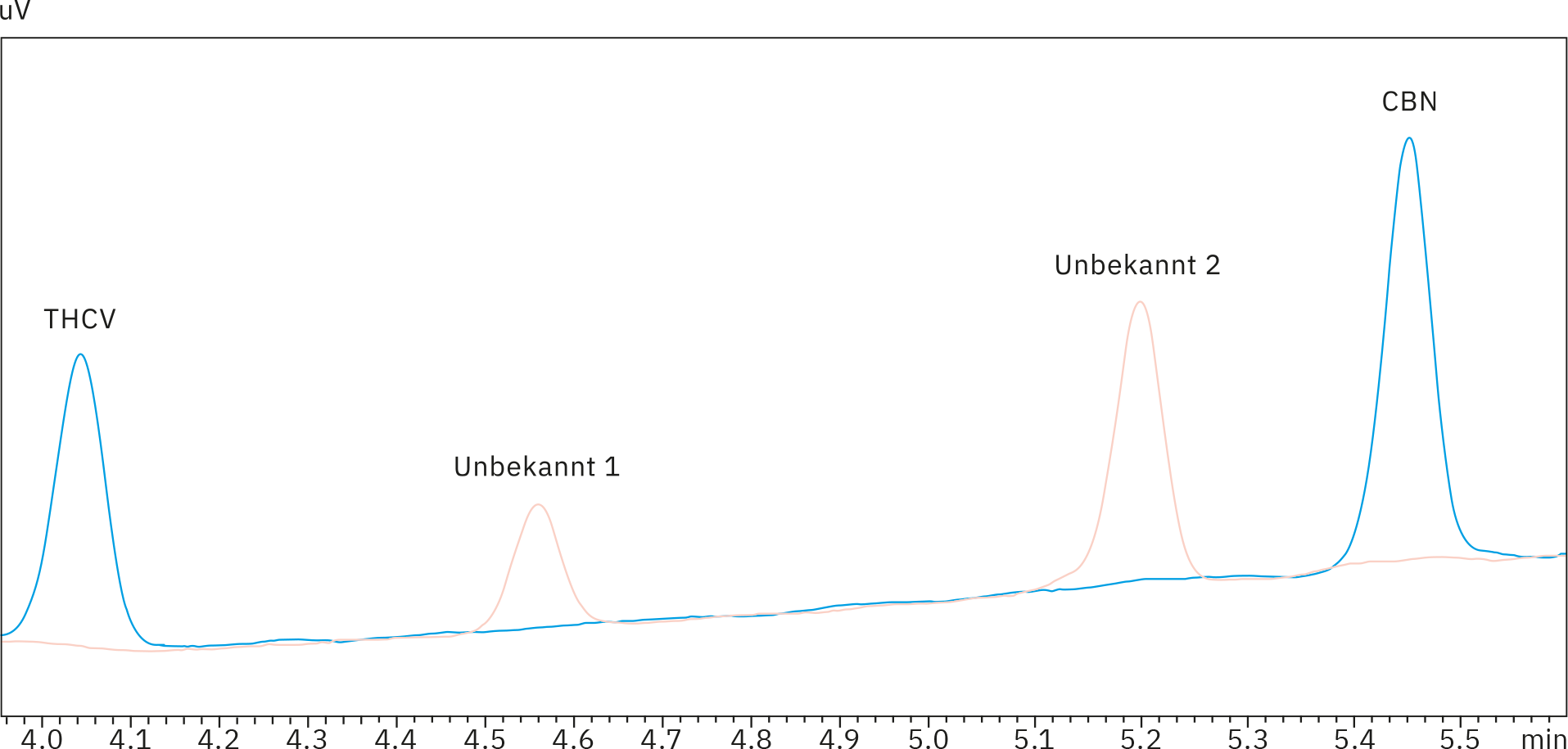
Zur Bestimmung der Selektivität des Tests wurden sämtliche Gummiprodukte auf unbekannte Peaks neben den 11 Cannabinoiden untersucht. In allen Chromatogrammen unterschiedlicher Konzentrationen war ein Signal bei einer Retentionszeit (tR) von 3,88 min zu sehen. Es wurde festgestellt, dass es ca. 0,05 ppm CBD entspricht, also deutlich unter dem niedrigsten Standard.
Die Gummiproben 4, 6, 7 und 8 wiesen außerdem Peaks bei 4,52 und 5,15 Minuten auf, die sehr wahrscheinlich auf den gelben Farbstoff im Produkt zurückzuführen sind, der allen vier Extrakten gemeinsam war. Da jedoch diese beiden Signale, die zwischen den Peaks von THCV und CBN lagen, deutlich von allen anderen Stoffen von Interesse getrennt waren, werden sie keine Fehlinterpretationen oder Einordnungsprobleme verursachen. Referenzprobe 4 wies unbekannte Peaks bei tR = 4,52 und 5,15 min auf, die jedoch in der Standardlösung von 0,5 ppm nicht vorhanden waren, wie aus den beiden übereinander gelegten Chromatogrammen hervorgeht (Abbildung 4).
Mit dem hochempfindlichen Verfahren wurden weitere Präzisionsproben analysiert, die mit Lösung (B) versetzt waren, zur Bestimmung aller 11 Cannabinoide. Aufgrund der geringeren Konzentration der unbedeutenderen Cannabinoide in den Proben war hier der zusätzliche Verdünnungsschritt nach der Extraktion nicht erforderlich (Abb. 3).
Tabelle 3 zeigt die durchschnittlichen Wiederfindungsergebnisse und die %RSD für die Extraktion der beiden Proben zur Beurteilung der Präzision des Verfahrens für alle 11 Cannabinoide.
|
Cannabinoid |
Durchschnitts- |
% Nennwert |
% RSD |
|
CBDV |
1,976 |
98,8 |
0,465 |
|
CBDA |
2,032 |
101,6 |
1,427 |
|
CBGA |
2,030 |
101,5 |
0,627 |
|
CBG |
1,997 |
99,9 |
0,637 |
|
CBD |
2,033 |
101,7 |
0,835 |
|
THCV |
1,983 |
99,1 |
1,177 |
|
CBN |
1,969 |
98,4 |
1,401 |
|
D9-THC |
2,025 |
101,2 |
0,873 |
|
D8-THC |
1,967 |
98,3 |
1,043 |
|
CBC |
1,971 |
98,6 |
0,359 |
|
THCA |
2,008 |
100,4 |
0,493 |
Die drei ausgewählten, handelsüblichen Produkte wurden extrahiert und auf alle 11 Cannabinoide untersucht. In Probe 1 und 2 wurden die 10 unbedeutenderen Cannabinoide mit Hilfe des unverdünnten Extrakts (A) bestimmt. CBD wurde in der Verdünnung bestimmt (4 x wie in Abbildung 3 dargestellt). Da Probe 3 eine geringere Menge an CBD aufwies, wurden alle Cannabinoide mit Hilfe des unverdünnten Extrakts (A) bestimmt. Die Ergebnisse der Bestimmung des Cannabinoid-Gehalts in handelsüblichen Proben sind in den Tabellen 4–6 aufgeführt.
|
Ergebnis (mg/g) |
||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
CBDV |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
|
CBDA |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBGA |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBG |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBD |
4,490 |
4,923 |
4,812 |
4,783 |
4,839 |
4,959 |
4,614 |
4,681 |
|
THCV |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBN |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
|
D9-THC |
— |
— |
— |
— |
— |
— |
— |
— |
|
D8-THC |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBC |
— |
— |
— |
— |
— |
— |
— |
— |
|
THCA |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
< 0,5 |
|
Ergebnis (mg/g) |
||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
CBDV |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
|
CBDA |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBGA |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBG |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBD |
4,541 |
4,463 |
4,294 |
4,548 |
4,550 |
4,124 |
4,595 |
4,520 |
|
THCV |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBN |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
|
D9-THC |
— |
— |
— |
— |
— |
— |
— |
— |
|
D8-THC |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBC |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
|
THCA |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
<0,5 |
|
Ergebnis (mg/g) |
||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
CBDV |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBDA |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBGA |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBG |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBD |
0.903 |
0.608 |
0.733 |
0.677 |
0.726 |
0.713 |
0.968 |
0.637 |
|
THCV |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBN |
— |
— |
— |
— |
— |
— |
— |
— |
|
D9-THC |
— |
— |
— |
— |
— |
— |
— |
— |
|
D8-THC |
— |
— |
— |
— |
— |
— |
— |
— |
|
CBC |
— |
— |
— |
— |
— |
— |
— |
— |
|
THCA |
— |
— |
— |
— |
— |
— |
— |
— |
Da CBD der einzige Peak in dem Konzentrationsbereich war, der in allen drei Proben festgestellt wurde, erfolgte die statistische Analyse nur von CBD von den acht Extraktionen (Tabelle 7).
|
Probe Nr. |
Durchschnitt |
Standard- |
% RSD |
mg/Gummi |
% Nennwert |
|
1 |
4,762 |
0,159 |
3,33 |
9,51 |
95,1 |
|
2 |
4,454 |
0,162 |
3,64 |
18,86 |
94,3 |
|
3 |
0,746 |
0,126 |
16,91 |
2,41 |
48,2 |
Es wurden auch weitere Informationen zu den Gummis berücksichtigt. Die Konzentration wird auf handelsüblichen Produkten im Allgemeinen als mg/Gummi oder mg/Beutel unter Angabe der Anzahl der Gummiprodukte angegeben. Dementsprechend wurde die Analyse durch Wiegen von 10 Stück jeder Probe durchgeführt, um ein Durchschnittsgewicht der Gummis zu erhalten.
Probe 1 – 19,9713 g/10 Gummis [10 mg/Gummi]
Probe 2 – 42,3488 g/10 Gummis [20 mg/Gummi]
Probe 3 – 32,2951 g/10 Gummis [5 mg/Gummi]
Die in Tabelle 7 aufgeführten Ergebnisse beinhalten auch die Ergebnisse für mg/Gummi und % Nennwert laut Packungsangabe.
Fazit
Die hochempfindliche Methode von Shimadzu für Wirksamkeitstests auf der i-Serie LC-2060 mit Photodioden-Array (PDA)-Detektor ist ein sehr robustes Verfahren für die exakte Bestimmung des CBD-Gehalts. Eine einfache Lösungsmittelextraktion erfordert wenig zusätzliche, für die Probenvorbereitung notwendige Laborausrüstung.
Auswertungen der Extraktion von Gummibärchen nach Standardaddition lieferten genaue Daten mit guter Wiederfindungsrate (über 98 %, < 1,5 %RSD für alle Cannabinoide). Ferner hat die Verwendung von handelsüblichen Produkten gezeigt, dass das Extraktionsverfahren für vegane und nicht vegane Süßigkeiten geeignet und zweckmäßig ist. Eine Probe (Probe 3) ergab niedrige prozentuale Nominalwerte in Verbindung mit einer hohen %RSD. Es konnte gezeigt werden, dass diese Probe kein homogenes Produkt war und Schwankungen als Folge des Herstellungsverfahrens aufwies.
Referenzen
- Shimadzu Corporation, Application News No. HPLC-016, Potency Testing in Cannabis Extracts Using a High Sensitivity Method with the Cannabis Analyzer for Potency, February 2017