Gemeinsam stärker
HPLC und SFC: Methodenentwicklung für chirale Verbindungen mit der Nexera SFC

Ein allgemeiner Überblick über die SFC-Technik: Wo sind ihre Unterschiede und Vorteile gegenüber der konventionellen UHPLC und woraus erwachsen Vorzüge im Zusammenspiel? Ein Umschaltsystem zwischen SFC und UHPLC bietet den Anwendern Flexibilität bei der Methodenentwicklung, wie anhand einiger Anwendungsbeispiele gezeigt. Insbesondere zur Trennung einer chiralen Verbindung wird oft eine SFC eingesetzt. Hierzu wird eine Applikation für ein Arzneimittel entwickelt sowie für eine Verbindung, die sich als Startsubstanz für zukünftige organische Synthesen verwenden lässt.
SFC – „grüne“ Technologie
Die Chromatographie mit überkritischen Fluiden (supercritical fluid chromatography = SFC) ist eine Trenntechnik, die als primäre mobile Phase eine superkritische Flüssigkeit einsetzt. Da superkritische Fluide eine geringere Viskosität und ein höheres Diffusionsvermögen haben als übliche Flüssigkeiten, führen sie zu einem niedrigeren Säulen-Gegendruck als bei der UHPLC-Trennung. Das bedeutet, dass sie sich für eine Hochgeschwindigkeits- und eine hohe Trennrate bei hohen Flussraten nutzen lassen.
Üblicherweise wird superkritisches Kohlendioxid in der SFC eingesetzt. Seine Polarität ähnelt Hexan, einem gesättigten Kohlenwasserstoff. Da es schwierig ist, Zielsubstanzen unter alleiniger Verwendung von superkritischem Kohlendioxid von einer Säule zu eluieren, wird der mobilen Phase ein organisches Lösungsmittel als Modifizierungsmittel zugefügt. Dies verändert ihre Polarität, sodass sich die Zielsubstanzen von der Säule eluieren lassen.
Arzneimittel, Nahrungsmittel und Umweltprüfungen sowie viele andere Anwendungsfelder benötigen eine große Bandbreite an Trennmethoden, etwa zur Auftrennung von chiralen Verbindungen und Strukturisomeren. Aufgrund der unterschiedlichen Trennselektivität der UHPLC und der SFC mithilfe von superkritischem Kohlendioxid sowie organischen Lösungsmitteln, wurden der SFC in den letzten Jahren große Erwartungen als neue chromatographische Trennmethode entgegengebracht.
Zudem lässt sich eine vorhandene UHPLC-Anlage mit spezifischen Geräten zu einem UHPLC/SFC-Umschaltsystem erweitern. Durch den Einsatz zweier Trennverfahren für das Screening während der Methodenentwicklung, gelingt es mit dem System, schneller bessere analytische Bedingungen zu konfigurieren. [1] SFC ist auch als „grüne“ Technologie bekannt, da an Verbrauch und Entsorgung organischer Lösungsmittel gespart wird.
Unterschiede zwischen HPLC- und SFC-Trenncharakteristiken
Die SFC-Säuleneffizienz nimmt sogar bei hohen Flussraten nicht so stark ab wie bei der HPLC. Daher ermöglicht die SFC eine Hochgeschwindigkeitsanalyse und kürzere Analysezeiten, kann aber zu einer anderen Elutionsreihenfolge und einer unterschiedlichen Trennselektivität führen. Die SFC kann sogar die Auftrennung derjenigen Verbindungen verbessern, die mit einer HPLC schwierig zu trennen sind.
- Kürzere Analysezeit: Durch eine geringe Viskosität und ein hohes Diffusionsvermögen des superkritischen Kohlendioxids, ist der SFC-Säulen-Gegendruck sogar bei hohen Flussraten gering, was eine Steigerung der Analysegeschwindigkeit erlaubt ohne Verlust der Säuleneffizienz. Wie Abbildung 1 zeigt, kann die SFC, bei Verwendung einer gepackten Säule mit der gleichen Partikelgröße wie bei der HPLC, drei- bis fünfmal kürzere Analysezeiten erreichen als die HPLC, ohne die Trennung zu gefährden.
- Elutionsreihenfolge: HPLC und SFC haben unterschiedliche Elutionscharakteristiken. Abbildung 2 zeigt HPLC- und SFC-Chromatogramme dreier Arten von Arzneimittelbausteinen. Sowohl für die HPLC als auch für die SFC wurde eine ODS-Säule eingesetzt, aber die Elutionsreihenfolge war unterschiedlich. Komponenten mit hoher Retention bei der HPLC werden bei der SFC schnell eluiert, was zu schärferen Peaks führt und daher einen hochempfindlichen Nachweis erlaubt. Die SFC ist auch nützlich, die Elutionsreihenfolge zu ändern bei Überlagerung durch kontaminierende Bestandteile.
- Verbesserte Trennselektivität: Da die SFC im Vergleich zur HPLC unterschiedliche Trennmuster aufweist, kann die SFC die Trennung zwischen Isomeren verbessern. Abbildung 3 zeigt den Vergleich einer HPLC- und SFC-Trennung bei Strukturisomeren. Die Triterpene, Oleanol- und Ursolsäure wurden mit der HPLC unzureichend getrennt, durch die SFC aber vollständig. Folglich lassen sich die Unterschiede in der Trennselektivität von HPLC und SFC effektiv dazu nutzen, die Trennung von Isomeren und Verunreinigungen zu verbessern, was zuvor schwierig war. [1]
UHPLC/SFC-Umschaltsystem
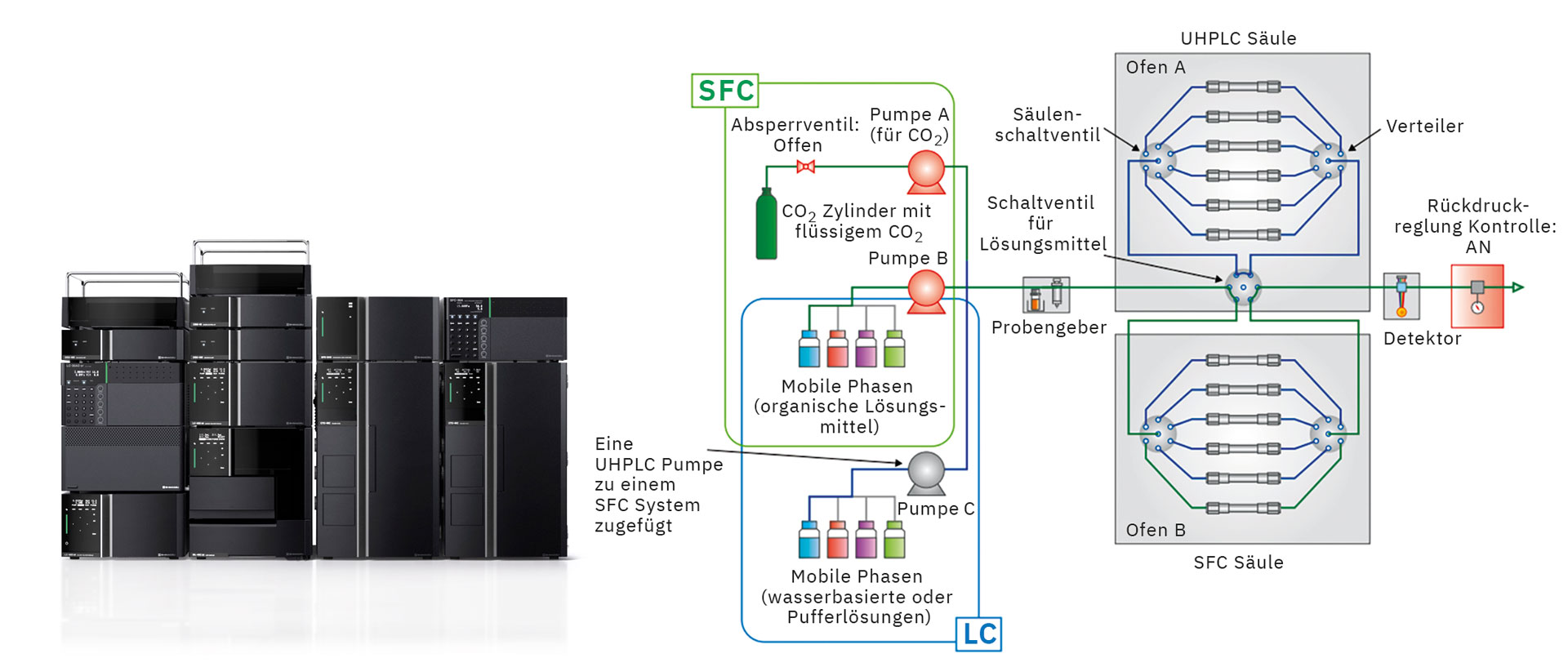
Berücksichtigt man die Trennbedingungen, können UHPLC und SFC dabei helfen, bessere Trennbedingungen zu ermitteln. Daher ermöglicht ein Nexera UC/s UHPLC/SFC-Umschaltsystem, den UHPLC- wie den SFC-Analysemodus in einem einzigen System zu nutzen. Abbildung 4 zeigt das Flussdiagramm.
Das System wurde zusammengestellt aus einer Standard-UHPLC-Anlage, kombiniert mit einer Einheit, die superkritisches Kohlendioxid zuführt, und einer Komponente zur Regulierung des Gegendrucks. Der UHPLC- wie der SFC-Analysemodus lassen sich durch Einschalten (Kontrollmodus ON oder OFF) der Kohlenstoffdioxidpumpe und Zuschalten des Gegendruckregulators nutzen. Die Pumpe (zum Einpumpen der organischen Lösungsmittel), den Autosampler, den Säulenofen und den Detektor gemeinsam für SFC wie UHPLC Analyse zu nutzen, minimiert den Raumbedarf wie auch die Ausstattungskosten und steigert die Nutzungsrate der Anlage.
Auch ein bestehendes UHPLC-System lässt sich zu dieser Anlage erweitern. Darüber hinaus lassen sich mit dem Lösungsmittelauswahlventil für die mobile Phase und dem Säulenschaltventil der Säulen automatisch die Bedingungen der mobilen Phasen ändern – für bis zu zwölf Säulen, um eine Vielzahl an Bedingungen zu ermöglichen, was die Effizienz der Methodenentwicklung verbessert. [1]
SFC-Anwendungsentwicklung für chirales Boc-DL-Phenylalanin und Cinacalet-HCl [2]
Boc-DL-Phenylalanin ist eine chirale Aminosäure, die sich als Ausgangsstruktur für eine zukünftige organische Synthese einsetzen lässt, woraus später Produkte in der Pharma- oder Chemieindustrie resultieren. Cinacalet ist ein Arzneimittel und wird in der EU unter dem Markennamen MIMPARA® verkauft, um Erkrankungen der Nebenschilddrüse zu behandeln, etwa primären und sekundären Hyperparathyreoidismus oder Tumore. Die chemischen Strukturen sind in Abbildung 5 dargestellt.
Als Ausgangspunkt zur Verfahrensentwicklung wird eine aus der Literatur bekannte HPLC-Normal-Phase-Applikation herangezogen; siehe Abbildung 7 für Boc-DL-Phenylalanin [3] und Abbildung 8 für Cinacalet-HCl. [4]
Methodenbedingungen für Abbildung 7
| Säule: | Chiralpak IA 250 mm x 4,6 mm, 5,0 µm |
| Mobile Phase: | Hexan/Isopropanol 4:1 mit 0,1 % TFA |
| Flussrate: | 1,0 ml/min |
| Temperatur: | 25 °C |
| Detektion: | PDA @220 nm |
Methodenbedingungen für Abbildung 8
| Säule: | Chiralpak IA 250 mm x 4,6 mm, 5,0 µm |
| Mobile Phase: | Hexan/Ethanol 95:5 mit 0,1% TFA |
| Flussrate: | 1,0 ml/min |
| Temperatur: | 25 °C |
| Detektion: | PDA @223 nm |
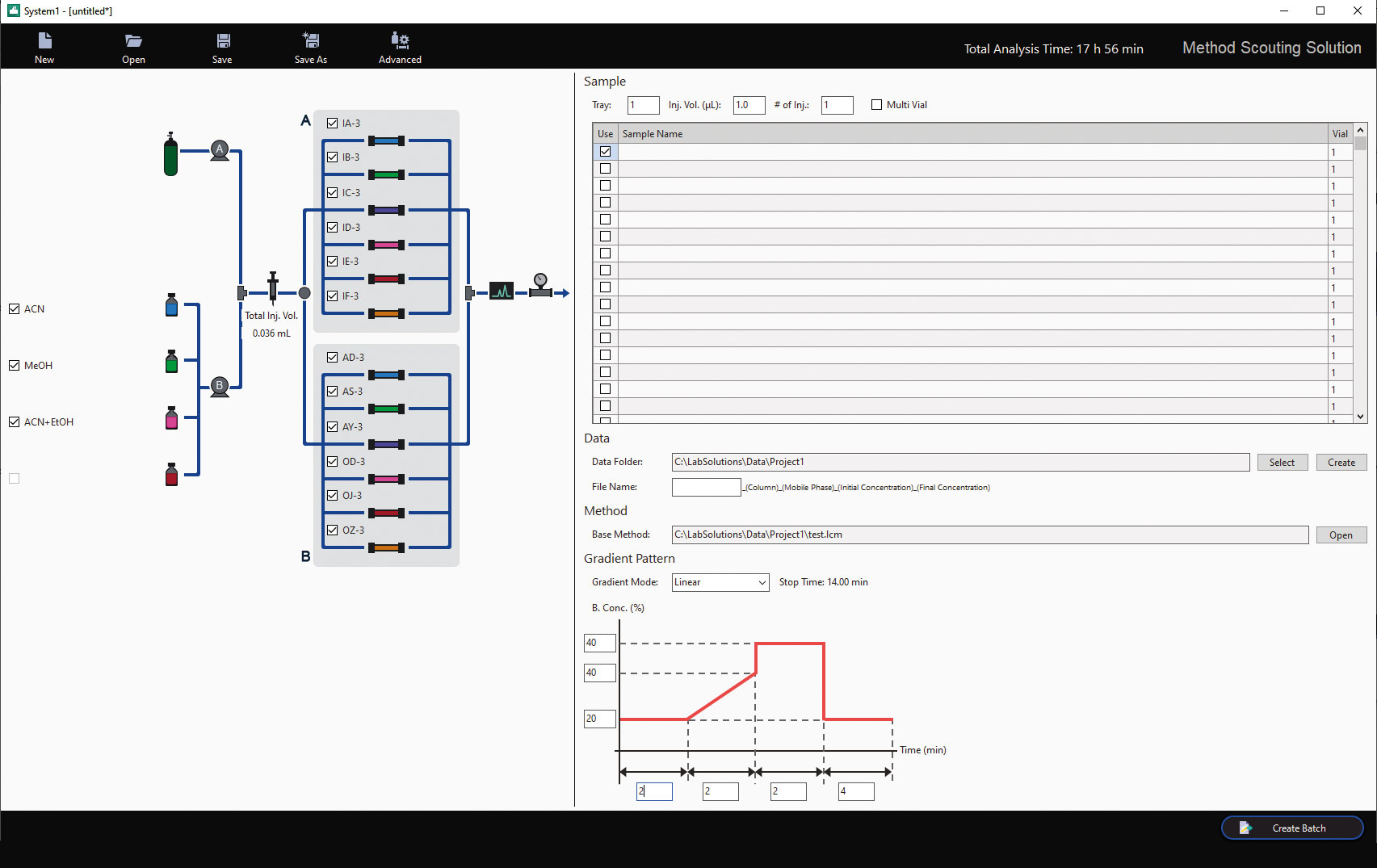
Unter Einsatz des SFC-Teils des Nexera UC/s UHPLC/SFC-Umschaltsystems und mit Hilfe der Method-Scouting-Software lässt sich eine neue Methode leicht entwickeln (siehe Abbildung 6). Die Software wurde konzipiert, um menschliche Fehler beim Verfassen von Methoden zu verhindern und diesen Prozess zu automatisieren. Für Scouting-Durchläufe wurde eine Kombination von vier verschiedenen Modifikatoren (Methanol, Ethanol, Isopropanol und Acetonitril) mit zwei Additiven (0,1 % TFA – Trifluoressigsäure, 0,1 % DEA – Diethylamin) und 10 DAICEL-Säulen (Chiralpak IA, IB, IC, ID, IE-3, AD-H, AS-H, AY-H und Chiralcel OD-H, OJ-H, OZ-3) getestet. Diese Kombinationen ergeben insgesamt 120 Durchläufe und die besten Trennkombinationen werden für eine weitere Verbesserung wie Gradienten- oder Flussrateneinstellungen verwendet.
Für die Verbindung Boc-DL-Phenylalanin wird das Chromatogramm in Abbildung 9 und für die Substanz Cinacalet-HCl das Chromatogramm in Abbildung 10 als einsatzbereites SFC-Verfahren vorgestellt.
Methodenbedingungen für Abbildung 9
| Säule: | Chiralpak AD-H 150 mm x 4,6 mm, 5,0 µm |
| Mobile Phase A: | CO2 |
| Mobile Phase B: | 0,15 % Diethylamin in Methanol |
| Gradient: | B konz. 2 % (0 min) → 20 % (10-11 min) →2 % (11,01-20 min) |
| Flussrate: | 2,0 ml/min |
| Temperatur: | 40 °C |
| Injektionsvolumen: | 5 µl |
| BPR: | 150 bar |
| BPR-Temperatur: | 50 °C |
| Detektion: | PDA @220 nm |
Methodenbedingungen für Abbildung 10
| Säule: | Chiralpak AY-H 250 mm x 4,6 mm, 5,0 µm |
| Mobile Phase A: | CO2 |
| Mobile Phase B: | Methanol/Isopropanol 1:1 mit 0,15 % Diethylamin |
| Gradient: | isocratisch mit 10 % B konz. |
| Flussrate: | 1,7 ml/min |
| Temperatur: | 40 °C |
| Injektionsvolumen: | 5 µl |
| BPR: | 220 bar |
| BPR-Temperatur: | 50 °C |
| Detektion: | PDA @220 nm |
Fazit
Das Nexera UC/s UHPLC/SFC-Umschaltsystem ermöglicht sowohl eine UHPLC- als auch eine SFC-Analyse, ohne die Flusslinie zu verändern. Das Verfahren zur Methodenermittlung mit der Methoden-Scouting-Software, die das Umschalten zwischen dem UHPLC- und SFC-Modus unterstützt, lässt sich dazu einsetzen, automatisch eine Sequenz zu erzeugen und auszuführen, die für die Umschaltmodi benötigt wird. Dazu gehört u.a. das Purgen der mobilen Phase, die im vorangegangenen Modus verwendet wurde, und das Spülen der Flusslinien mit der mobilen Phase, die für den nächsten Lauf benötigt wird. Somit besteht keine Notwendigkeit, komplizierte Prozesse durchzuführen, wie z.B. die Erzeugung von Methoden für jede Kombination von Säule und mobiler Phase.
Durch einfache Festlegung von (1) mobilen Phasen, (2) Säulen, (3) Proben, (4) der Basismethode für die Analyse und (5) Gradientenbedingungen (Ausgangskonzentration, Endkonzentration und Gradient) kann die Software automatisch eine Batch-Tabelle für den Einsatz des Methoden-Scoutings generieren. Dies stellt sicher, dass sogar Erstanwender problemlos das automatische Umschalten zwischen UHPLC und SFC nutzen und einfach eine Methode mit beiden Techniken übertragen und entwickeln können, wie an zwei Anwendungsbeispielen zur Trennung chiraler Verbindungen gezeigt.
www.shimadzu.eu/sfc-uhplc-switching-system
Literatur
- Hidetoshi Terada, Takato Uchikata, Keiko Matsumot, Tadayuki Yamaguchi, Yasuhiro Funada, Technical Report C190-E212, First Edition: December 2018
- Silvan Buholzer, Diplomarbeit Titel: Trennung chiraler Moleküle mittels überkritischer Flüssigkeitschromatographie, Februar 2021
- Y. Komaravolu, V. R. Dama, T. C. Maringanti, Anal. Methods 2018, 10, 2481-2493
- V. Ravinder, S. Ashok, M. Satish Varma, C. V. Raghunath Babu, K. Shanker, G. Balaswamy, Chromatographia 2009, 70, 229-232