DOSIURA™ – eine neue Lösung für das Screening auf DPD-Mangel
Messung von Uracilämie mittels LC-MS/MS als präziser Ansatz
Sibylle Collard, Julia Petit, Mikael Levi, Alsachim
Die europäischen Gesundheitsbehörden empfehlen dringend, Patienten, die eine Chemotherapie auf Fluoropyrimidin-Basis benötigen, auf einen Mangel an Dihydropyrimidin-Dehydrogenase (DPD) zu screenen. In einigen Fällen ist dies sogar vorgeschrieben, um das Risiko schwerer Arzneimitteltoxizitäten zu reduzieren, die diese Behandlungen verursachen können. Eine indirekte Bestimmung des DPD-Mangels erfolgt durch die Messung der Uracil- und Dihydrouracilspiegel im Plasma. Zum leichteren Nachweis von DPD-Mangel bietet das DOSIURA™-Reagenzien-Kit eine gebrauchsfertige Analyselösung mit allen erforderlichen Reagenzien für die präzise Quantifizierung dieser Verbindungen mittels LC-MS/MS.
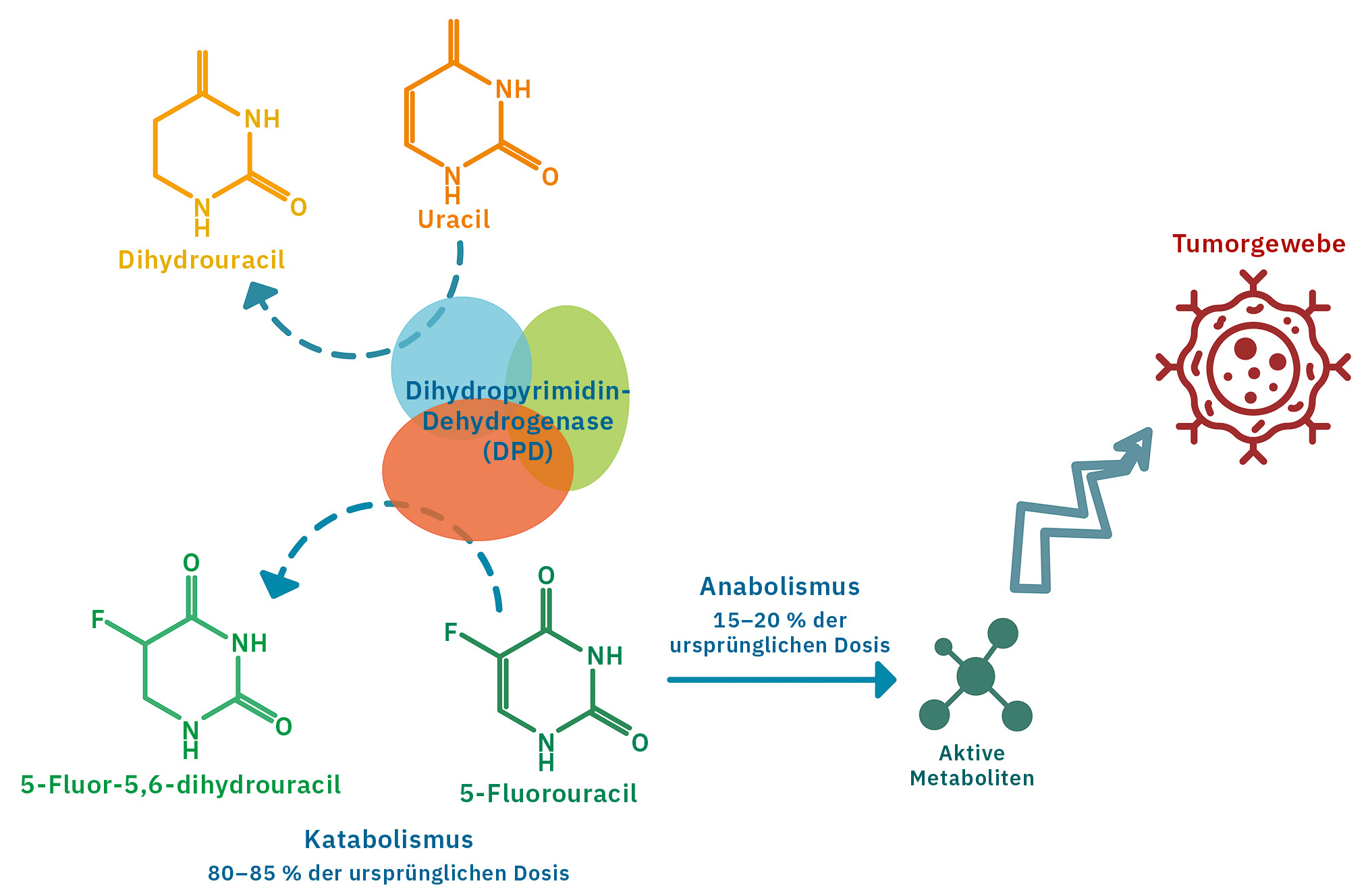
Fluoropyrimidine, eine Gruppe von Krebsmedikamenten, zu denen auch 5-Fluorouracil (5-FU) gehört, werden häufig zur Behandlung solider Tumore wie kolorektaler, Magen-, HNO- und Mammakarzinome eingesetzt. Allerdings können fluoropyrimidinbasierte Chemotherapien zu schweren Nebenwirkungen führen. Diese treten in einem von fünf Fällen auf und können schwere Toxizitäten (Grad 3–4 nach der WHO-Klassifikation der Chemotherapie-Toxizitäten) und selten, aber dennoch gelegentlich Todesfälle (Inzidenz zwischen 0,1 und 1 %) zur Folge haben.[1] Diese Toxizitäten könnten mit einem Aktivitätsmangel des wichtigsten am Abbau von 5-FU beteiligten Enzyms, der Dihydropyrimidin-Dehydrogenase (DPD), zusammenhängen (Abbildung 1).
Das Enzym DPD unterstützt den Körper beim Abbau von körpereigenen Pyrimidinen (Uracil und Thymin) und fluorierten Pyrimidinen wie 5-FU. Bei geringer Aktivität oder einem Mangel an DPD-Enzymen reichern sich diese Chemotherapeutika im Körper an und verursachen schwerwiegendere Nebenwirkungen als erwartet. Die 5-FU-Behandlung von Patienten mit einem ausgeprägten DPD-Mangel ist mit einem erhöhten Toxizitätsrisiko verbunden. Die DPD-Aktivität ist von Patient zu Patient unterschiedlich, weshalb es wichtig ist, vor Beginn der Behandlung abzuklären, ob ein Mangel vorliegt.
Mittlerweile empfehlen oder fordern viele Gesundheitsbehörden in Europa sowie weltweit eine systematische Untersuchung auf DPD-Mangel bei Patienten, die eine Chemotherapie mit Fluoropyrimidinen erhalten.
Test auf DPD-Mangel durch Genotypisierung oder Phänotypisierung
Bei der Genotypisierung handelt es sich um die Suche nach Varianten des DPYD-Gens, das das DPD-Enzym kodiert, während die Phänotypisierung die direkte oder indirekte Messung der Aktivität des Enzyms bedeutet.
Die Genotypisierung basiert derzeit auf der Suche nach vier Varianten: DPYD*2A, DPYD*13, c.2846A>T und HapB3. Damit lassen sich zwar Mängel feststellen, es werden jedoch nicht alle Populationen erfasst.[1] Außerdem wurden im Rahmen von Studien zahlreiche Toxizitäten festgestellt, die sich nicht durch Mutationen dieser vier Varianten erklären lassen.
Die alternative Methode der Phänotypisierung beruht auf der direkten Messung der DPD-Aktivität in PBMCs (mononukleären Zellen des peripheren Blutes) oder der indirekten Messung durch Quantifizierung der Uracil- und Dihydrouracilspiegel im Plasma. Die direkte Messung der Enzymaktivität ist jedoch äußerst komplex und zeitaufwendig, weshalb die indirekte Phänotypisierung bevorzugt wird. Die Plasmakonzentrationen dieser beiden Verbindungen werden durch Flüssigchromatographie in Kombination mit Tandem-Massenspektrometrie (LC-MS/MS) bestimmt.
DOSIURA™ – eine gebrauchsfertige Lösung für die schnelle Quantifizierung von Uracil und Dihydrouracil
Alsachim, ein Unternehmen der Shimadzu Gruppe, hat DOSIURA™ entwickelt, eine gebrauchsfertige Lösung für die Quantifizierung von Uracil und Dihydrouracil im Plasma zur schnellen Bestimmung eines DPD-Mangels. Dieses innovative Reagenzien-Kit und seine Analysemethode bieten eine Lösung für viele der Probleme, mit denen Labors und Krankenhäuser bei der Phänotypisierung von DPD-Mangel konfrontiert sind.
Die Empfehlungen für ein präventives Screening auf DPD durch Gesundheitsbehörden wie der Europäischen Arzneimittelagentur (EMA) ab 2020,[2] der ANSM in Frankreich und der MHRA in Großbritannien stellen Krankenhäuser und biomedizinische Labors vor eine doppelte Herausforderung: eine erhöhte Nachfrage nach Analysen auf DPD-Mangel [3] und die Notwendigkeit, langwierige und hochkomplexe Probenvorbereitungs- und Analysemethoden zur Durchführung dieser Analysen zu entwickeln.
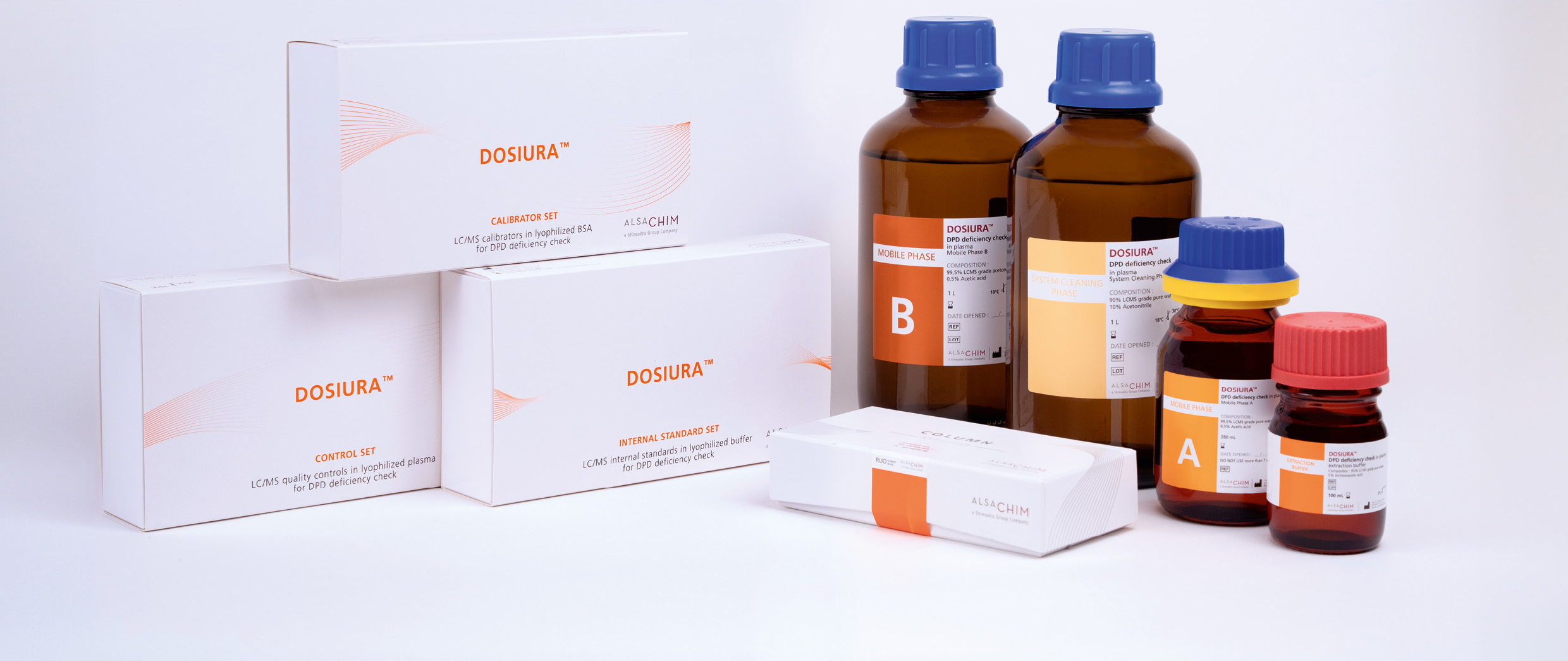
DOSIURA™, die einzige auf dem Markt erhältliche Lösung dieser Art
Das Kit ermöglicht die schnelle Messung von Uracil und Dihydrouracil basierend auf dem zuverlässigeren und reproduzierbaren Ansatz der indirekten Phänotypisierung und der LC-MS/MS-Methode für die gleichzeitige Quantifizierung mehrerer Verbindungen.
DOSIURA™ enthält die Qualitätsreagenzien, die für diese Analysen benötigt werden: Kalibriermittel, interne Standards (synthetisiert von den Chemikern von Alsachim) und Kontrollen zur Vermeidung von Komplexität und analytischer Instabilität, die mit der Reagenzienvorbereitung für Labors verbunden ist. „Die Kontrollen werden in echtem Humanplasma hergestellt und in Konzentrationen formuliert, die als Entscheidungsgrundlage für die Beurteilung des DPD-Mangels dienen. Dies erleichtert dem Kliniker die Entscheidungsfindung nach der Analyse der Ergebnisse“, erklärt Julia Petit, Projektleiterin im Bereich Forschung und Entwicklung bei Alsachim.
DOSIURA™ ist eine Komplettlösung mit den erforderlichen Verbrauchsmaterialien und einer robusten Analysemethode:
- Drei Sets bestehend aus Kalibratoren mit sechs Stufen und Leerwert, mit stabilen Isotopen, markierten internen Standards und Qualitätskontrollen mit drei Stufen
- Gebrauchsfertige Reagenzien: mobile Phasen und Reinigungsphase, Extraktionspuffer und analytische Säule
- Probenvorbereitungsprotokoll und analytische Parameter sind bereits festgelegt
Uracil und Dihydrouracil sind polare endogene Verbindungen mit niedrigem Molekulargewicht, weshalb sich die Methodenentwicklung für das F&E-Team als große Herausforderung erwies, insbesondere die Abtrennung der Zielverbindungen von allen in der Matrix vorhandenen interferierenden Molekülen. „Unser Ziel war es, unseren Kunden eine schnelle, genaue und zuverlässige Lösung zu bieten“, so Julia Petit.
Die DOSIURA™-Lösung gewährleistet die messtechnische Rückverfolgbarkeit dieser Verbindungen und eine besonders zügige Probenvorbereitung: Das Protokoll und die mitgelieferten Reagenzien ermöglichen eine schnellere Probenvorbereitung im Vergleich zu bereits verfügbaren Methoden.[4, 5] „Wir wollten eine schnelle Komplettlösung für die Probleme anbieten, die sich in Krankenhäusern und Labors ergeben. Das Screening auf DPD-Mangel ist ein wichtiges Thema. Mit DOSIURA™ können wir die Forschung zur Behandlung von Krebspatienten unterstützen und unseren Kunden ein wichtiger Partner bei ihrer täglichen Arbeit sein.“
Gewährleistung einer sicheren Krebsbehandlung
Angesichts der zunehmenden Verbreitung des Screenings auf DPD-Mangel in Ländern weltweit und des Inkrafttretens der IVDR und ihrer Anforderungen an Medizinprodukte und die Standardisierung von Methoden kann DOSIURA™ einen wichtigen Beitrag zur routinemäßigen und schnellen Analyse von Uracil- und Dihydrouracilkonzentrationen leisten.
DOSIURA™ ist nur für Forschungszwecke und nicht zur diagnostischen Verwendung vorgesehen.
[1] Recherche de déficit en dihydropyrimidine déshydrogenase en vue de prévenir certaines toxicités sévères survenant sous traitement comportant des fluoropyrimidines (5-fluorouracile). Recommandations et référentiels. INCa. HAS. December 2018, updated September 2023.
[2] Fluorouracil and fluorouracil related substances (capecitabine, tegafur and flucytosine) containing medicinal products. Assessment report. EMA/274404/2020.
[3] de With, M., Sadlon, A., Cecchin, E., Haufroid, V., Thomas, F., Joerger, M., van Schaik, R.H.N., Mathijssen, R.H.J., Largiadèr, C.R. ‘The Working Group on the Implementation of DPD-deficiency Testing in Europe’ (Apr 2023). Implementation of dihydropyrimidine dehydrogenase deficiency testing in Europe. ESMO Open. 8 (2): 101197. doi: 10.1016/j.esmoop.2023.101197. Epub 2023 Mar 28. PMID: 36989883. PMCID: PMC10163157.
[4] Tafzi, N., Woillard, J.B., Fleytoux, A., Picard, N., Marquet, P. (Aug 2020). Phenotyping of Uracil and 5-Fluorouracil Metabolism Using LC-MS/MS for Prevention of Toxicity and Dose Adjustment of Fluoropyrimidines. Ther Drug Monit. 42 (4): 540–547. doi: 10.1097/FTD.0000000000000768. PMID: 32384537.
[5] Coudoré, F., Roche, D., Lefeuvre, S., Faussot, D., Billaud, E.M., Loriot, M.A., Beaune, P. (Nov–Dec 2012). Validation of an ultra-high performance liquid chromatography tandem mass spectrometric method for quantifying uracil and 5,6-dihydrouracil in human plasma. J Chromatogr Sci. 50 (10): 877–84. doi: 10.1093/chromsci/bms085. Epub 2012 Jun 11. PMID: 22689904.